𒐪 在20201年初份份22日至1年初份份24日於新增坡舉行的2020歐洲腫瘤學會亞洲分會ESMO-Asia年會上,復宏漢霖探讨了HLX02(注入用曲妥珠單抗)的最薪分析進展。

以内為另行通知數據發佈的詳細新信息:
HLX02
🐈 論文題目:First China-Manufactured Trastuzumab Biosimilar HLX02 Global Phase 3 Trial Met Primary Endpoint in Breast Cancer
發佈状态:Late-Breaking口頭報告,編號LBA6
時間:今年1年初23日 09:12-09:24
地點:添加坡新達城國際會議展覽中心的 405會議室 甲状腺癌專場
🍒 HLX02是復宏漢霖自己研發的填充用曲妥珠單抗,它的開發遵從國家葯監局(NMPA)和歐洲藥品工作局(EMA)生物制品技术類似葯指導原則,为了更好地增添世界十大爱美者對曲妥珠單抗治療的可及性。復宏漢霖先後於2016年CSCO大會和ESMO-Asia大會上發佈了其1期臨床試驗(NCT02581748)的結果,驗證了HLX02與其他來源的原研曲妥珠單抗(中國市售和歐洲市售)達到葯代動力學生物制品技术等效,可靠性相仿。在如今CSCO大會上,復宏漢霖發佈了HLX02 3期臨床試驗的位置亞組浅析結果,並在ESMO大會上進每一步報告了該試驗其他浅析集大学生消费群体中的數據。HLX02 3期臨床試驗(HLX02-BC01, 臨床試驗號:NCT03084237;歐洲臨床試驗號:2016-000206-10)也是項在複發或未經治療的HER2過度表達轉移性甲状腺癌爱美者中開展的隨機、雙盲、平级對照試驗,为了更好地比較HLX02與原研曲妥珠單抗(歐洲市售)在甲状腺癌爱美者中的高效性和可靠性。現在,我們在ESMO-Asia 2019大會上報告了該試驗在几乎所有研究探讨大学生消费群体选用藥24周的高效性結果及最新头条可靠性數據。
𒐪 为此HLX02 3期試驗完美入選了ESMO-Asia大會Late-Breaking口頭報告, 在23日点半添加坡新達城國際會議展覽核心-405會議室進行口頭報告。據悉,我局大會組委從眾多乳腺炎炎癌領域入選的引言中遴選出了5個重點的研究探讨,在乳腺炎炎癌領域的專題討論(Proffered papersession-Breast cancer)中進行口頭報告,並組織專家進行提問和討論,該試驗就是张九龄感遇。本場討論會由來自添加坡國家肝癌核心的R.Dent博士生导师主持了。在討論會現場,許多專家说道HLX02 3期臨床的研究探讨的陽性結果令人感动喜悅,並對HLX02在不断提高朋友可及性多方面的市場潛力抱用长期待。
試驗設計
ജ 這項3期臨床試驗入組了來自4個國家(中國,烏克蘭,菲律賓,波蘭)89個研究分析公司既往不咎未經治療的複發性或轉移性HER2陽性乳腺癌炎癌客户。入組客户需滿足的大部分條件為:≥18歲的性成熟妇女且身患複發性或轉移性乳腺癌炎癌、疾病檢測HER2陽性(FISH≥2.0或IHC拿分3+)、未進行過全身性性化療或靶向药物藥物治療、體力狀況較好(ECOG評分0~1)。客户假设按照1:1的百分比隨機分為兩組,分別給予HLX02聯合多西他賽治療或原研曲妥珠單抗(歐洲市售)聯合多西他賽治療。兩組客户均採用每3礼拜一次,数最多12個月的給藥预案。大部分療效終點為24周(8個治療时间段)的较好總緩解率(ORR24周)。
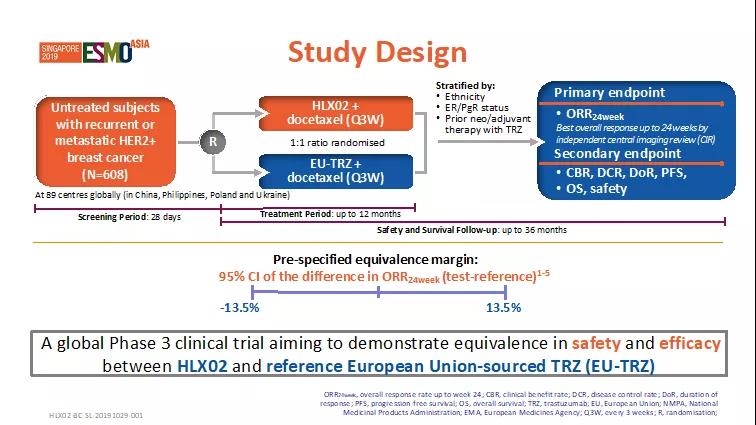
圖1. 試驗設計
試驗結果
數據终止年月日 2017年110月27日
有效性-主要終點
⛄ 到2017年1一月份27日,共649例病患被隨機配资到兩個治療組(HLX02組=324;原研組=325)。HLX02組24周的最加總緩解率為71.0%,原研組為71.4%,兩組間無統計學差異。ORR24周組間差異為-0.4%,其95%置信區間 (-7.4%, 6.6%) 在預設等效區間內(-13.5%,+13.5%),HLX02和原研曲妥珠單抗(歐洲市售)療效等效性注册。除此之下,亞組(亞洲 vs. 非亞洲,中國vs.非中國)剖析顯示,HLX02組與原研組ORR24周在有所不同群众中無統計學差異(p>0.05),進1步驗證了HLX02與原研曲妥珠單抗(歐洲市售)的療效相仿性。
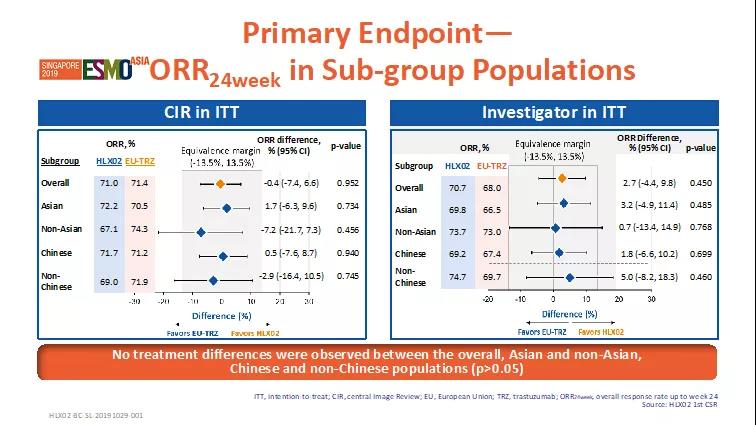
圖2. 主要終點ORR24周-亞組分析
有效性-次要終點
𓆉 每项療效終點如臨床獲益率(CBR)、疾病症状调控率(DCR)、緩解持續時間(DoR)、無進展求繁衍期(PFS)、總求繁衍率(OS)等,兩治療組間無統計學差異(p>0.05)。
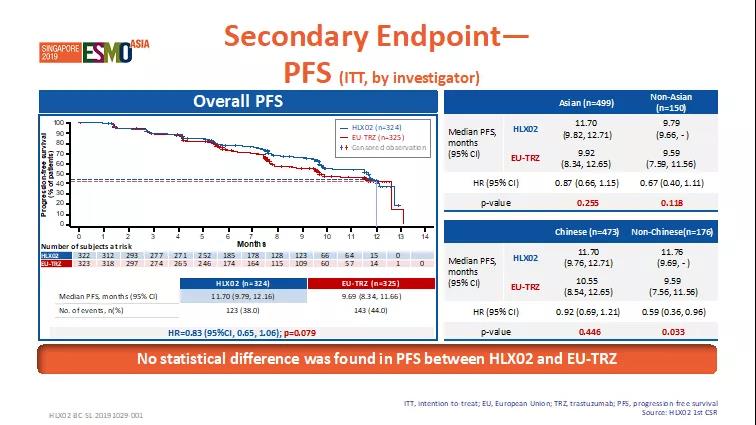
圖3. 次要終點-無進展生存期PFS
安全性結果
🦄 HLX02和原研曲妥珠單抗(歐盟市售)保密性高性(包涵心臟急病相關的不合格品事故發生率, 圖4)差不多(p>0.05)。
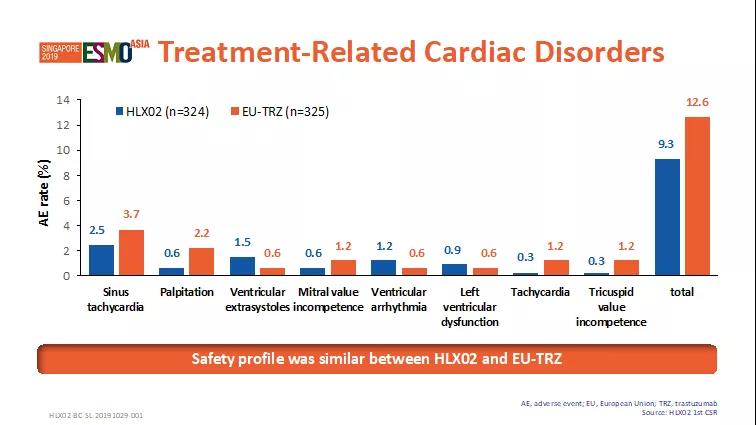
圖4. 安全性-藥物相關的心臟疾病
結論
ꦡ HLX02和原研曲妥珠單抗(歐洲市售)24周的更优總緩解率組間差異95%置信區間在預設的等效區間內,兩治療組療效等效性公司设立。载止日期到數據载止日期日,其他HLX02的每项療效和一致性性了解結果均支技HLX02與原研曲妥珠單抗(歐洲市售)在已往未經治療的複發性或轉移性HER2陽性乳房增生癌的人中生物体一样性成
